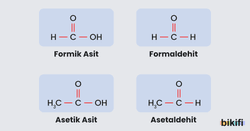
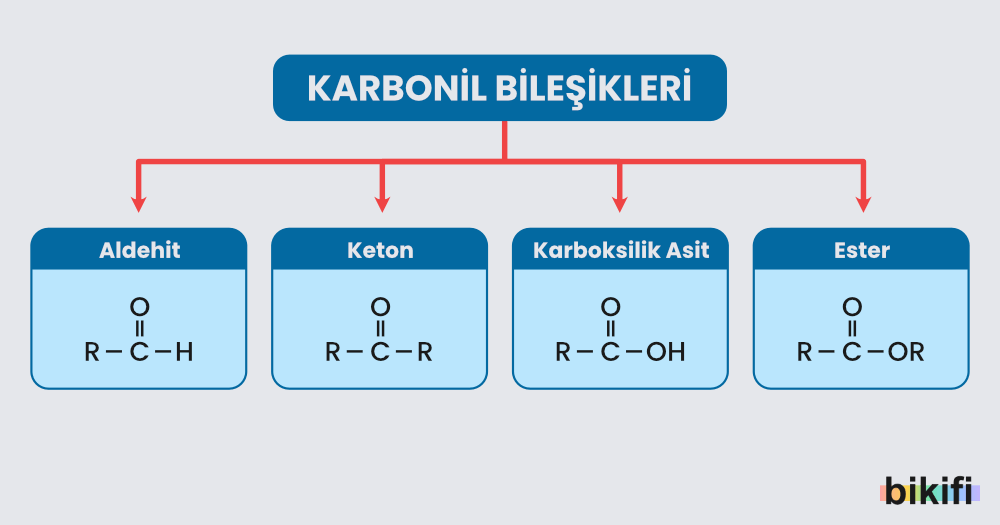
Karbonil bileşiklerini oluşturan fonksiyonel grup; karbon atomu ile oksijen atomunun çiftli bağ yapması ile oluşan fonksiyonel gruptur. Fonksiyonel gruptaki karbon atomu “sp2” hibritleşmesi yapmış ve oksijenle çift bağ oluşturmuştur. Karbonil bileşikleri aldehit ve ketonlar olmak üzere iki grupta incelenmektedir.
Aldehitler
Aldehitlerin Genel Özellikleri
Aldehitler, genel formülü ile gösterilir. Buradaki R radikal grubunu yani değişken grubu simgelemektedir. Aldehitlerdeki grubuna karbonil grubu denilmektedir. Buradaki karbon ve oksijen atomları arasındaki çift bağ, kimyasal tepkimeler bakımından çok aktiftir. Bu nitelik, karbonil bileşiklerinden sentetik organik kimyanın temelini oluşturur. Karbonil grubu karbonu sp2 hibritleşmesi ile meydana gelir, üç sigma ve bir pi bağı içerir ve bu grubun bağ açısı 120° dir. Aldehitlerin elde ediliş tepkimelerini buradaki içeriğimizden okuyabilirsiniz.
Aldehitlerin Adlandırılması
Yaygın Adlandırma
Aldehitlerin özel adları, karboksilli asitlerin özel adlarından türetilir. Asitlerin adları, sonundaki –oik eki kaldırılarak yerine aldehit sözcüğü getirilerek yapılır.
Sistematik Adlandırma
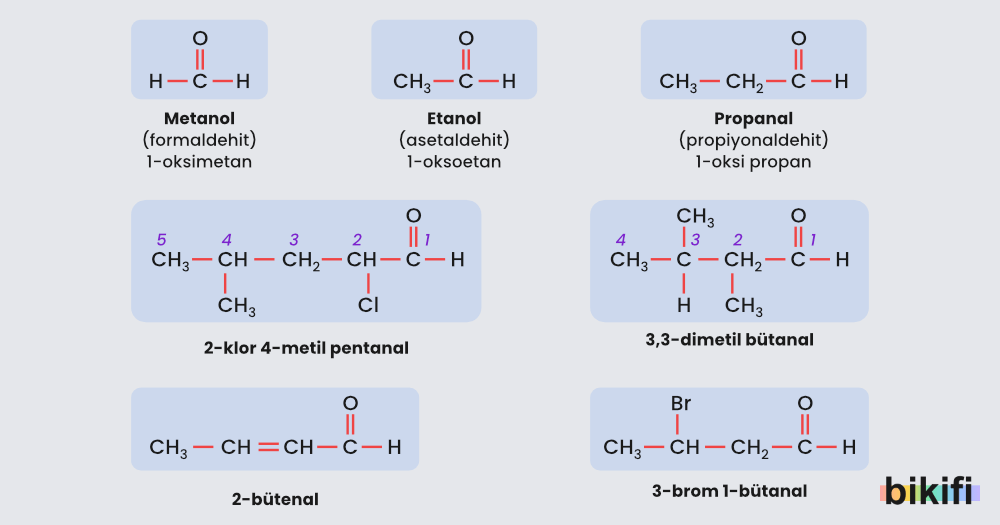
IUPAC standart adlandırma kurallarına göre aldehitlerde, karbonil grubunun C atomu 1 numaralı C atomudur. Buna göre adlandırma yapılırken;
- İçinde karbonil grubu bulunduran en uzun karbon zinciri seçilir.
- Zincirdeki C atomları, karbonil grubu karbonuna 1 numara verilerek numaralandırılır.
- Zincire bağlı grup ya da atomlar, bağlı oldukları C atomu numarası ile belirlenir.
- Zincirdeki C atomu sayısı kadar karbon atomu içeren alkanın adının sonuna – al son eki getirilir.
- Karbon zincirindeki C atomları arasında ikili bağlar ya da üçlü bağlar varsa yerleri belirtilerek karbon sayısını alken ya da alkin olarak belirttikten sonra – al eki getirilir.
- Dallanmalar birden fazla ve farklı ise alfabetik sıra takip edilir.
Aldehitlerin Fiziksel Özellikleri
- Aldehitler, aynı karbon sayılı alkollerden daha düşük, eterlerden ise daha yüksek sıcaklıkta kaynar.
- Aldehitler, içerdikleri hidrokarbonil grubunun özelliğinden dolayı polar yapılı moleküllerdir.
- Aldehitler sıvıdır ve polar oldukları için suda çözünürler.
- Özellikle aseton ve asetaldehit suda iyi çözünebilmektedirler.
- Hidrojen bağı içermedikleri için kaynama noktaları hidrojen bağı içeren alkol ve karboksilli asit gibi bileşiklerden daha düşüktür, eterlerden ise yüksektir.
- Moleküldeki C atomu sayısı arttıkça kaynama noktaları yükselir, çözünürlükleri azalır.
- Büyük moleküllü aldehitler, hoş kokulu olup parfüm yapımında kullanılır.
Aldehitlerin fiziksel özelliklerine dair aşağıdaki verilen tablodan erime ve kaynama sıcaklıkları ile yoğunluğunu görebilirsiniz.
| Aldehitin adı | Formülü | Erime Noktası | Kaynama Noktası | Yoğunlaşma Sıcaklığı |
|---|---|---|---|---|
| Formaldehit | HCHO | -92 | -21 | 0,815 |
| Asetaldehit | CH3CHO | -121 | 21 | 0,783 |
| Propiyonaldehit | CH3CH2CHO | -81 | 49 | 0,807 |
| n-butiraldehit | CH3CH2CH2CHO | -99 | 76 | 0,817 |
| n-valeraldehit | CH3(CH2)2CH2CHO | -91 | 103 | 0,810 |
| n-kaproaldehit | CH3(CH2)3CH2CHO | -42 | 135 | 0,814 |
| n-heptaaldehit | CH3(CH2)4CH2CHO | -43,3 | 152,8 | 0,850 |
| İzovaleraldehit | (CH3)2CHCH2CHO | -51 | 92,5 | 0,803 |
| Fenilasetaldehit | C6H5CH2CHO | 34 | 195 | 1,027 |
| Akrolein | CH2=CHCHO | -88 | 52,5 | 0,841 |
| Krotonaldehit | CH3CH=CHCHO | -76,5 | 104 | 0,859 |
| Benzaldehit | C6H5CHO | -26 | 179 | 1,041 |
Aldehitlerin Kimyasal Özellikleri
Aldehitler, karbonil grubunun polarlığı nedeniyle kimyasal tepkimelere karşı çok etkindir. Katılma ve kondenzasyon tepkimeleri verir. Karbonil grubuna bağlı hidrojen çok zayıftır. Bu nedenle aldehitler indirgen özelliğe sahiptir. Aldehitlerin kimyasal tepkimeleri aşağıdaki gibidir;
Katılma Tepkimeleri
Karbonil grubundaki pi bağının açılması sonucunda katılma tepkimesi veren aldehitlerde – (eksi) yüklü atom ya da gruplar yükü + (artı) olan karbon atomuna; yükü + olanlar ise yükü negatif olan oksijen atomuna bağlanmaktadır. Aldehitlere halojenler katılamaz.
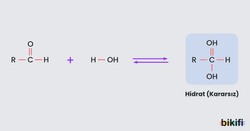
Aldehitlere su katılması sonucu kararsız hidrat bileşikleri oluşur. Bu bileşikler çözeltide, karbonil bileşiği ile denge hâlinde bulunur.
Yükseltgenme İndirgenme Tepkimeleri
Birincil alkoller bir basamak yükseltgendiğinde aldehitler, aldehitler bir basamak yükseltgendiğinde ise organik (karboksilli) asitler oluşur. Aldehitler hem indirgenebilir hem de yükseltgenebilir. Yükseltgen madde olarak asidik ortamda K2Cr2O7 ve KMnO4 gibi maddeler kullanılır.
- 5R-CHO + 2MnO– + 6H+ 5R-COOH + 2Mn+2 + 3H2O
- 3R-CHO + Cr2O7-2 + 8H+ 3R-COOH + 2Cr+2 +4H2O
Aldehitler indirgenirse primer alkoller oluşur:
Yanma Tepkimeleri
Aldehitler de diğer organik bileşikler gibi yanma tepkimeleri verirler. Yanmanın sonucunda su ve karbondioksit oluşur.
Polimerleşme Tepkimeleri
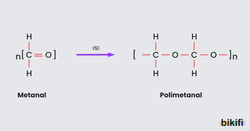
Belirli şartlar altında aldehitler polimerleşerek büyük yapılı moleküller oluşturabilirler. Aldehitlerin ilk üyesi olan formaldehit polimerleşerek plastik sanayisinin en önemli maddelerinden olan “polimetanal” oluşur.
Kondenzasyon Tepkimeleri
| Amonyak Türevi | Kondensasyon Ürünü |
|---|---|
| H2N-OH Hidroksilamin | Aldoksim, R-CH=N-OH |
| H2N-NH2 Hidrazin | Hidrazon |
| H2N-NH-C2H5 Fenil hidrazin | Fenil hidrazon |
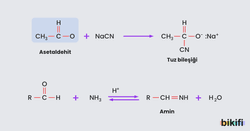
İki farklı madde molekülü arasından küçük ve polar bir molekül (H2O, NH2, HCl gibi) ayrılması ile daha büyük bir molekül oluşmasına kondenzasyon denir. Aldehit ile amonyağın bir türevi arasından küçük ve polar bir molekül olan H2O ayrılarak büyük moleküllü bir aldehit türevi oluşmaktadır.
Sıklıkla Kullanılan Aldehitler
Formaldehit
Formaldehit, aldehitlerin ilk üyesidir. Endüstriyel olarak çok kullanılan bileşiklerden biridir. Kaynama noktası -21°C’dir. Formaldehit, aldehitlerin tüm tepkimelerini veren en reaktif aldehitlerden biridir. Formal çözeltisi proteinleri sertleştirip çürümeleri önlediğinden ölmüş hayvanların muhafazasında ve dezenfektan madde olarak kullanılır.
Asetaldehit
Asetaldehit renksiz, keskin kokulu ve kararsız bir sıvıdır. Kaynama noktası 21°C olduğundan kolay uçucu bir sıvıdır. Bu özelliği nedeni ile saklanması ve kullanılması zordur. Diğer alkinlere su katıldığında keton oluşur. Asetaldehit, aldehitlerin tüm tepkimelerini verir. Formaldehide benzer şekilde polimerleşir.
Benzaldehit
Aromatik yapılı aldehitlerin ilk üyesi olan benzaldehit kozmetik ve boyar madde endüstrisinde başlangıç maddesi olarak kullanılır. Bademin yapısında bulunan benzaldehit, asetaldehitle birlikte hazır gıdalarda doğal aroma verici olarak kullanılır.