Karbon atomları arasında tekli bağ bulunduran doymuş hidrokarbonlara ‘Alkan’ denilmektedir. Genel formülleri CnH2n+2dir. Tepkimeye girme istekleri az olduğundan alkanlara “etkinliği az” anlamına gelen Latince kelime olan parafin de denilmektedir.
Alkanların en küçük üyesi olan metan hayatımızın birçok alanında karşımıza çıkar. Evlerimizde kullandığımız tüplerde, petrol türevlerinin içerisinde veya bataklık, lağım, kömür yataklarında bulunabilmektedir. Genellikle biyolojik etmenlerin sonucunda doğada bulunabilir. Örneğin bitkisel maddelerin bozunması sonucunda doğada kömür yüksek basınç ve sıcaklık altında kaldığında ise elmas gibi maddeler olarak rastlanabilmektedirler.
Alkanlar düz zincirli, dallanmış ve halkalı yapıda olabilir. Alkanların yapısındaki bütün bağlar sigma bağıdır ve yapısındaki bütün karbon atomları sp3 hibritleşmesi yapmıştır.
Alkanların Adlandırılması
Organik bileşiklerde sayısız molekül bulunmaktadır. Bu moleküllerin sistematik bir biçimde adlandırılması gerekmektedir. Sistematik olarak yapılan adlandırmaya bilimsel adlandırma denilir. Organik kimyada genellikle bilimsel adlandırma kullanılır (bazı molekülleri çok uzun zamandır tanıdığımız ve kullandığımız için eski adları kullanılabiliyor, bu tarz isimlendirmeye yaygın adlandırmadenilmektedir).
Organik bileşiklerin adlandırılması International Union of Pure and Applied Chemistry (Uluslararası Kuramsal ve Uygulamalı Kimya Birliği) kurallarına göre yapılır. Kısa adı IUPAC olan bu kurumun organik bileşiklerin adlandırılması için kabul ettiği bazı sayılar ve bu sayıların Latince okunuşları tabloda gösterilmiştir.
| Sayı | Latince Okunuşu |
|---|---|
| 1 | Mono |
| 2 | Di |
| 3 | Tri |
| 4 | Tetra |
| 5 | Penta |
| 6 | Hekza |
| 7 | Hepta |
| 8 | Okta |
| 9 | Nona |
| 10 | Deka |
Alkanların Bilimsel Adlandırılması
Hidrokarbonları bilimsel olarak adlandırırken öncelikli olarak aşağıdaki tablo bilinmelidir.
Alkanların ilk dört üyesinin özel adı vardır. Diğer alkanlarda ise karbon sayısını gösteren rakamın sonuna -an eki getirilerek okunur.
| Adı | Formulü |
|---|---|
| Metan | CH4 |
| Etan | C2H6 |
| Propan | C3H8 |
| Bütan | C4H10 |
| Pentan | C5H12 |
| Hekzan | C6H14 |
| Heptan | C7H16 |
| Oktan | C8H18 |
| Nonan | C9H20 |
| Dekan | C10H22 |
Bir moleküldeki bütün bağların açık şekilde yazıldığı formüle yapı formülü (açık formül) denir. Karbonlar ile hidrojenler arasındaki bağların gösterilmediği yapı formülüne yarı açık formül denir. Karbonlara bağlı grupların karbon atomundan sonra yazıldığı, aralarındaki bağların gösterilmediği formüle sıkıştırılmış yapı formülü denir
Alkanlar bilimsel olarak adlandırılırken aşa�ğıdaki adımlar sırasıyla uygulanır.
- Kesintisiz en uzun karbon zinciri seçilir. Bu zincirdeki karbon sayısına denk gelen alkanın adı esas alınır (tabloya bakabilirsiniz). Örneğin 7 karbonlu bir zincirde adlandırma yapılırken heptan olarak sonuna ekleriz.
- En uzun karbon zinciri, dallanmaya yakın uçtan numaralandırılmaya başlanır. Görsel 1’deki örnekte görüldüğü gibi birden fazla dallanma olduğunda dallanmanın en yakın olduğu yerden numaralandırılmaya başlanmaktadır.
- Ana zincirde birden fazla yan grup varsa iki uçtan başlanıldığı zaman karşılaşılan ilk yan gruba bakılır. İlk yan gruplar ana zincirin uçlarına eşit mesafede ise ikincilere, onlar da eşitse diğerlerine bakılır.
- Dallanmanın bağlı olduğu karbona verilen numara yazılır ve araya tire (-) konulur daha sonra dallanmanın adı belirtilir. Dallanmaların sırası alfabetik şekilde olmalıdır. Görsel 2 de örnek olarak 3–brom–4–etil–2 metil bileşiği verilmiştir.
- Aynı cinsten birden fazla dallanma varsa yunanca sayısı di(2) , tri(3) ,tetra(4) , penta (5) vb. şeklinde belirtilir. Görsel 3’te örnek olarak 2,2,4–trimetil bileşiği verilmiştir.
- En uzun karbon zincirine karşılık gelen alkanın adı adlandırmanın sonuna eklenir. Örnek olarak görsel 4’te 4–etil–2,6–dimetil heptan bileşiği verilmiştir.

Alkanların Özel (Yaygın) Adlandırmaları
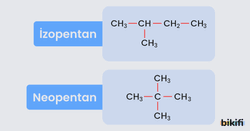
İzo ve Neo ön ekleri ile adlandırma yapılırken dikkat edilecek hususlar şöyledir;
Alkan molekülünde ana zincirde 2.karbon atomuna bir metil(CH3) bağlı ise “izo” ön eki alır, eğer iki tane metil (CH3) grubu bağlı ise “neo” ön eki alır. Örneğin 2-metil propan molekülünün yaygın adı “İzobütan”dır.
🚨 Dikkat: -izo ve -neo adlandırmalarında moleküldeki tüm karbon atomlarının sayılarak alkanın adının belirlendiğine dikkat etmeliyiz.
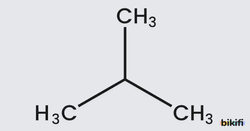
İzobütan (2-metil propan) bileşiği aşağıda verilmiştir.
Karbon atomuna sadece başka bir karbon atomu bağlıysa karbon atomuna primer (birincil) karbon atomu, karbon atomuna iki ayrı karbon atomu bağlıysa karbon atomuna sekonder (ikincil) karbon atomu, karbon atomuna üç ayrı karbon atomu bağlıysa karbon atomuna tersiyer (üçüncül) karbon atomu denir.
Bir alkanın hidrojen atomları, bağlı oldukları karbon atomları esas alınarak sınıflandırılır. Birincil karbon atomuna bağlı hidrojen atomu birincil (1o ) hidrojen atomudur. İkincil karbon atomuna bağlı hidrojen ikincil (2o ) hidrojen atomu ve üçüncül karbon atomuna bağlı hidrojen ise üçüncül (3o ) hidrojen atomudur.
Karbon sayısı 3 ve daha fazla olan alkanlardan hidrojen eksilmesi birden fazla şekilde gerçekleşebilir. Ayrılan hidrojenin türüne göre alkil grupları primer, sekonder ve tersiyer olarak sınıflandırılır.
Primer karbon atomundan hidrojen eksilirse primer alkil, sekonder karbon atomundan hidrojen eksilirse sekonder alkil ve tersiyer karbon atomundan hidrojen eksilirse tersiyer alkil grupları oluşur.
C3H8 (propan) bileşiğinin yaygın alkil türevleri aşağıda verilmiştir.
Halkalı Alkanların Adlandırılması
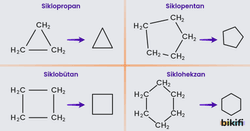
Organik kimyada çizgi halinde olmayan ve geometrik olarak başlangıcıyla sonu birbirine bağlanmış yapılara halkalı yapılar diyoruz ve bu yapıları isimlendirirken “siklo-” eki kullanıyoruz.
Sikloalkanların genel formülleri CnH2ndir. En küçük üyesi halkalı yapının oluşabilmesi için gerekli olan minimum değer olan 3 karbonludur. 3 karbonlu sikloalkanın adı ise “siklopropan“dır.
Adlandırmalarında halkalı olmayan alkanlara göre bir fark yoktur sadece karbon sayısına göre “-siklo” ön eki alır. Aşağıdaki tabloyu inceleyiniz.
Alkanların Özellikleri
Alkanların Genel Özellikleri
- Genel formülleri CnH2n+2olup bağ açısı 109,5° dir.
- VSEPR gösterimi AX4 tür ve düzgün dört yüzlü geometriye sahiptir.
- Halkalı alkanlarda halkadan dolayı iki tane hidrojen atomu eksilir ve genel formül CnH2nşeklinde olur.
- Eşit karbon sayılı hidrokarbonlar içerisinde hidrojen atom sayısı en fazla olan hidrokarbonlar alkanlardır.
Alkanların Fiziksel Özellikleri
- Alkanlar apolar bileşiklerdir. Bunun sonucu olarak moleküller arası çekim kuvvetleri (London kuvveti) görülmektedir. Molekülün büyüklüğü ve temas yüzeyi arttıkça London kuvvetleri artar.
- Alkan molekülleri arasında en etkili kuvvet “Wan der Walls” kuvvetleridir.
- Alkanlar apolar oldukları için suda yani polar çözücülerde çözünmezler. Buna karşın apolar olan çözücülerde (eter, benzen, CCl4 gibi) çözücülerde çözünürler.
- Alkanlarda molekül büyüklüğü arttıkça genellikle; yoğunluk, kaynama ve erime noktası artar, molekülde dallanma arttıkça kaynama ve erime noktası düşer.
- Tüm alkanların yoğunlukları 1 (g/ml) den küçük olduğu için su üzerinde yüzerler. Örneğin alkan yapıda olan petrol türevi benzinin yoğunluğu 0,750-0,850 (g/ml) dir.
Alkanların Kimyasal Özellikleri
- Alkanlar ve sikloalkanlar (halkalı alkanlar) diğer organik bileşiklere göre tepkimeye girmeye oldukça isteksizdir. Örneğin birçok organik bileşik kuvvetli asitlerle, bazlarla, yükseltgen ve indirgen maddelerle tepkime vermekteyken alkanlar bu maddelerle tepkime vermemektedirler.
- Alkanlara tepkimeye yatkın olmamaları nedeniyle Latince’de reaktivitesi az anlamına gelen “parafinler” adı verilmektedir.
Başlıca Alkan Kaynakları
Başlıca alkan kaynakları; petrol doğal gaz ve kömür yataklarıdır. Doğal gazın %60-90’ı kaynağına bağlı olarak metandan oluşmaktadır. CO2(karbondioksit) ve N (azot) , etan(C2H6) ve propan (C3H8) da içermektedir. Petrol “S” (Kükürt) ve “N” (Azot)’lu bileşikleri içeren alifatik ve aromatik bileşiklerin de bir kaynağıdır.
Alkanların Kullanım Alanları
Günümüzde daha çok yakıt olarak kullanılan alkanların ana kaynağı; petrol, kömür ve doğal gaz gibi fosil yakıtlardır. Alkanlar genellikle ham petrolün rafinerilerde damıtılmasıyla elde edilir.
Alkanlar çözücü olarak da yaygın şekilde kullanılır. Bir alkan bileşiği olan hekzan çok iyi bir çözücüdür. Bu nedenle laboratuvarlarda ve sanayide organik maddelerin çözünmesinde ve boyaların inceltilmesinde kullanılır.