Uzayda yer kaplayan her şeye madde denir. Maddeler kütleye ve hacme sahiptir. Maddeler belirli basınç ve sıcaklıklarda maddenin 4 temel halinden birisinde bulunabilir; katı, sıvı, gaz ve plazma. Maddeleri oluşturan moleküllerin davranışları maddenin her halinde değişiktir. Maddenin plazma halini şu yazımızda detaylıca okuyabilirsiniz.
Maddenin 3 Hali: Katı – Sıvı – Gaz
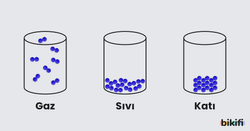
Maddenin katı, sıvı ve gaz hallerini kıyaslamamız gerekirse; genellikle katı maddeler maddenin en düzenli ve moleküllerin birbirine belirli bir düzende sıkı bir şekilde bağlandığını gözlemleriz. Moleküller arası bağlar sıvılarda şiddetini azaltır ve bu yüzden sıvıların belirli bir şekli bulunmaz. Gazlarda ise bu bağlar yok denecek kadar güçsüzleşir.
Kısacası moleküller arası bağların kuvveti maddenin katı, sıvı veya gaz halde bulunmasını etkiler. Bir maddenin molekülleri arasındaki bağ ne kadar güçlüyse kaynama ve erime sıcaklıklarını daha yüksek olur.
Suyun Özel Durumu
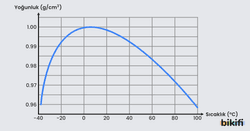
Bir maddenin katı, sıvı ve gaz halindeki yoğunlukları karşılaştırıldığında genellikle katı fazının en yoğun, gaz fazının en düşük yoğunluk durumda olması beklenir. Ancak suda bu durum beklenilen şekilde gözlemlenmemektedir.
Su, en yoğun haline sıvı haldeykenn ve +4.0 °C (deniz seviyesinde) de geçer. Buzun sudan daha az yoğunluğa sahip olmasının sebebi su katılaşırken moleküller arasında oluşan hidrojen bağının moleküller arası mesafeyi artırmasından kaynaklıdır. Oluşan bağ hacmi artırır ve yoğunluğun azalmasına neden olur. Bu durum (katı hale geçen suyun) buzun sıvısı üzerinde yüzmesine sebep olur. Böylece göller veya denizler donduğu zaman suyun altındaki yaşam soğuktan etkilenmeden devam eder.
Gaz Halinin Önemi ve Kimyasal Özellikleri
Gazlarda moleküller arası etkileşim çok az olduğu için sıkıştırılabilir. Bu sıkıştırılma özelliği sayesinde günlük hayatımızda kullandığımız deodorantları, evlerde kullandığımız tüpleri veya elektrik ürettiğimiz doğalgazı taşıyabilir ve istediğimiz zaman istediğimiz ölçüde kullanabiliriz.
Gazlar sıvılar içerisinde düşük sıcaklıklarda daha çok karışırlar. Bu nedenden dolayı içtiğimiz gazlı içeceklerin soğukluğuna bağlı olarak içindeki çözünen gaz miktarı değişkenlik gösterir. Eğer içeceğimiz daha soğuksa içerisinde daha çok gaz barındırır ve içeceğimiz daha lezzetli gelir. Ayrıca bazı gazlar klima gibi soğutucuların içerisinde kullanılır ve soğutma olayının gerçekleşmesini sağlar.