Sıvılar, maddenin temel hallerinden birisidir. Sıvıyı oluşturan moleküller arası çekim kuvveti, katılardan az gazlardan fazladır. Bu özelliği sayesinde katıların aksine sıvı moleküller birbiri üzerinde kayabilir yani akışkandır. Sıvılar zamanla birbirleri içinde dağılırlar, böylece bulundukları kabın şeklini alırlar.
Sıvının oluşmasını sağlayan moleküller arası çekim kuvveti, sıvıya başlıca buhar basıncı, viskozite ve yüzey gerilimi gibi bir çok özellik kazandırır.
Yüzey Gerilimi
Yüzey gerilimi, sıvılar da gözlemlenen kohezyon özelliği sayesinde meydana gelir. Sıvının sınırında bulunan sıvı molekülleri iç kısımlardaki moleküller tarafından çekilir. Bu da çok sayıda molekülün sıvı içine gitmesini, az sayıda molekülün yüzeyde kalmasını sağlar. Bunun sonucunda birbirine daha sağlam tutunan moleküller yüzeyde dirençli ve esnek bir katman oluşturur. Bu olaya yüzey gerilimi denir.
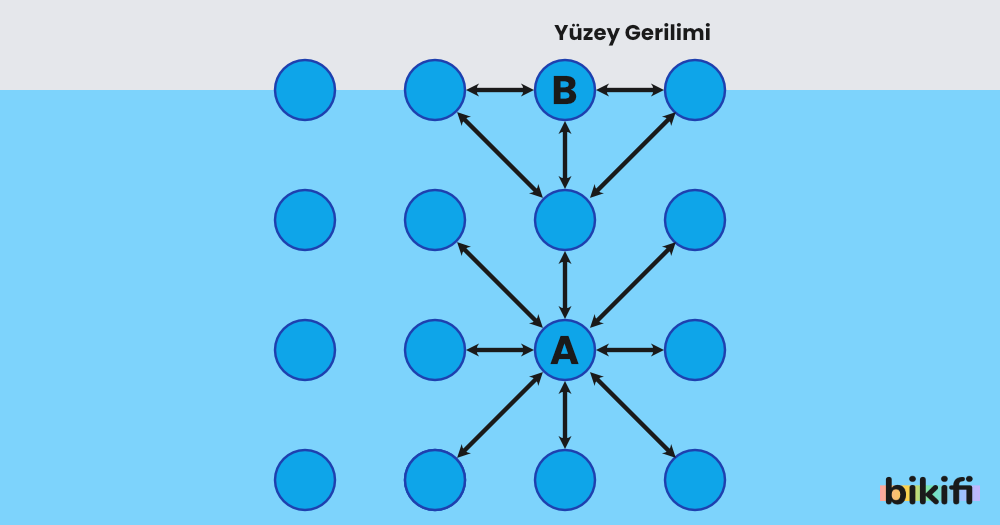
Havada bulunan bir su damlası yüzey geriliminin etkisiyle küresel olur, çünkü yüzeysel gerilimin oluşturduğu etki sıvıyı en düşük yüzey alanına sahip olacak yapıya sokar, bu yapı da küresel bir yapıdır. Yer çekiminin etkisiyle küresel şekil hafifçe düzleşebilir. Yüzey gerilimi hakkında daha fazla bilgi için tıklayın.
Kılcallık ile Yüzey Gerilimi Arasındaki İlişki
Kılcallık (veya diğer bir adıyla kapiler etki) sıvıların ince borular içinde yükselmesi ya da alçalmasına denir. Sünger gibi maddelerin suyu emmesi kılcallık etkisi sayesinde gerçekleşir. Silindirik bir boruda bir sıvının ne kadar yükseleceği ya da alçalacağı sıvının yüzey gerilim kat sayısı ile doğru orantılı; sıvının yoğunluğu, yer çekimi ivmesi ve borunun yarıçapı ile ters orantılıdır.
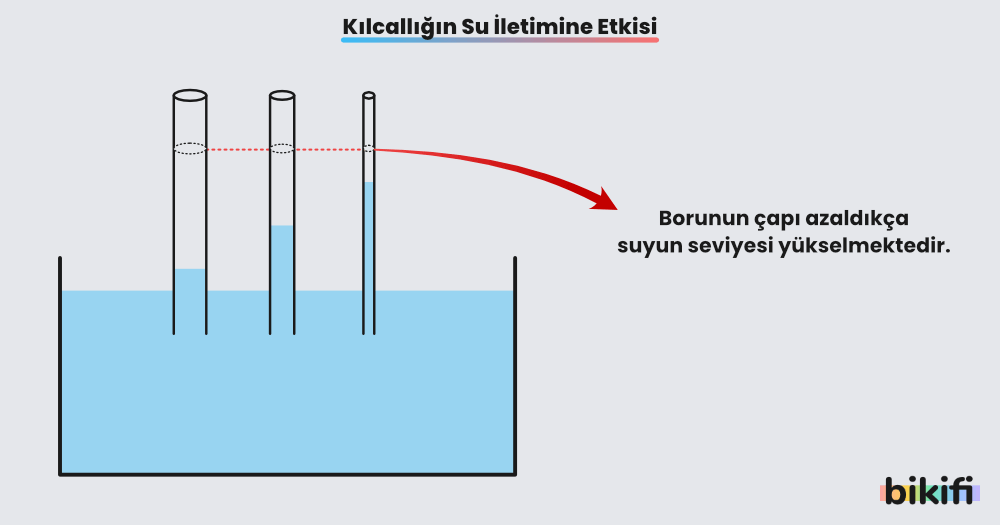
Kılcallık, adezyon ve kohezyon kuvvetleri sayesinde gerçekleşir.
Adezyon: Benzer olmayan moleküller arasındaki çekim kuvvetlerine adhezyon kuvvetler denir.
Kohezyon: Benzer tanecikler arasındaki çekim kuvvetlerine kohezyon denir.
Viskozite
Sıvıların akmaya karşı gösterdikleri dirence viskozite denir. Bir sıvının viskozitesi ne kadar fazla ise madde o kadar yavaş akar. Örnegin; yağ sudan daha viskoz bir sıvıdır. Yağın akışkanlığı sudan daha azdır. Moleküller arası etkileşim arttıkça sıvının viskozite özelliği de artar.
Buhar Basıncı
Bir maddenin sıvı halden gaz hale geçmesine buharlaşma denir. Sıvılarda gerçekleşen buharlaşma sıvı kaynarken net bir şekilde gözlemlenebilir.
!Not: İçerisinde gaz bulunan bir ortamda katılardan da buharlaşma gözlemlenir. Yine aynı koşullar sağlandıkça buharlaşma her sıcaklıkta gözlemlenir.
Dinamik Denge
Kapalı kap içerisine bir sıvı koyar ve yeteri kadar beklersek kabın içerisinde dinamik denge durumunu gözlemleriz. Bu gözlemin gerçekleşmesini 4 adıma ayırabiliriz.
- Belirli bir sıcaklığa (kinetik enerjiye) sahip sıvı buharlaşmaya başlar.
- Buharlaşma sırasında kapta bulunan gaz tanelerinin sayısı artar.
- Sayının artmasıyla birlikte gaz tanecikleri birbirleriyle çarpışarak kinetik enerjilerinin bir kısmını kaybeder ve tekrar sıvı hale dönerler (bu işleme yoğuşma denmektedir).
- Gaz tanecikleri sayısı belirli bir miktara gelince, buharlaşma ve yoğuşma işlemleri aynı hızda gerçekleşmeye başlar. Bu durumda dışarıdan gözlem yapıldığında buharlaşma durmuş gibi görünmesine karşın buharlaşma ve yoğuşma işlemleri devam eder. Bu duruma dinamik denge denir.
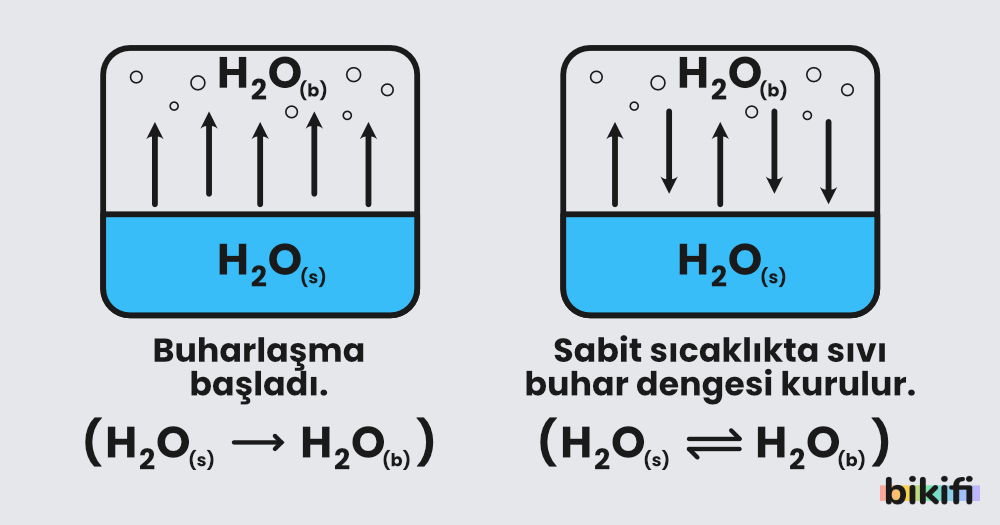
Sıvısıyla dengede olan buhar halinde bulunan moleküllerin belli bir sıcaklıkta yaptığı basınca sıvının buhar basıncı denir. “Devam yazısı: Buhar basıncını etkileyen faktörler“
Buhar Basıncı ile Kaynama Noktası Arasındaki İlişki
Sıvının sıcaklığı arttıkça buhar basıncı artar. Buhar basıncı, ortamdaki hava basıncına eşit olduğunda ise kaynama işlemi başlar. Kaynama işleminin başladığı sıcaklığa da kaynama noktası denmektedir. Kaynama sırasında sıvının sıcaklığı sabit kalır ve sıvıya ne kadar çok ısı verilirse sıvı o kadar hızlı buharlaşır. Bilimsel olarak kaynama noktaları, sıvının buhar basıncının 1 atm’e (760 mmHg) eşit olduğu sıcaklık alınır ve normal kaynama noktası olarak adlandırılır.
Buhar basıncının artması sıvının kaynama noktasını düşürür. Bu yüzden buhar basıncını etkileyen faktörler (sıvının cinsi ve sıvının saflığı ayrıntılar) kaynama noktasına da etki eder. Örneğin makarna yapılırken başlangıçta suya atılan bir tatlı kaşığı tuz, suyun daha geç kaynamaya başlaması için atılır. Daha geç kaynayan tuzlu su, yemeği daha çabuk pişirir.
Kaynama noktası ayrıca açık hava basıncından etkilenir. Açık hava basıncı, deniz seviyesinden yükseklere doğru çıkıldıkça azalır. Bu yüzden kaynama noktası azalır. Bunun en güzel örneği yemek pişirilirken gözlemlenir. 5000 m yükseklikte su 83°C sıcaklıkta kaynar ve suyun kaynaması ile yapılan yemekler (örneğin makarna) sıvının daha az ısı vermesinden dolayı daha geç pişer.
Yemeklerde oluşan bu durumu aşmak için düdüklü tencerelerde üretilmiştir. Düdüklü tencereler havayı içerisinde tutarak tencerenin içerisindeki hava basıncını arttırır. Böylece sıvı daha yüksek sıcaklıklarda kaynamaya başlar ve yemekler daha çabuk pişer.













