Metallerin parlaklık, tel ve levha hâline getirilebilme, ısı ve elektriği iyi iletme gibi ortak özellikleri vardır. Bu özellikleri açıklayan en temel konulardan biri “metalik bağ”dır. Metalik bağ, metal atomlarının birbirine uyguladığı çekim kuvvetini ve bu atomların bir arada durma biçimini açıklar.
Metalik Bağın Tanımı ve Temel Özellikleri
Metalik bağ, metallerin katyonik (pozitif yüklü) çekirdekleri ile bu çekirdeklerden koparak serbestçe dolaşabilen elektronlar arasındaki elektrostatik çekim kuvvetidir. Bu bağ, metallere aşağıdaki özellikleri kazandırır:
- Elektrik iletkenliği: Serbestçe hareket edebilen elektronlar sayesinde metaller, elektrik akımını kolaylıkla iletir.
- Isı iletkenliği: Hareketli elektronlar, ısı enerjisini de hızlıca iletebilir.
- Tel ve levha hâline getirilebilme (sünek ve dövülebilir olma): Metal atomları, yapılarındaki serbest elektronlar sayesinde kayma düzlemleri boyunca kolayca hareket edebilir. Böylece metaller tel hâline çekilebilir ya da ince levhalar hâline dövülebilir.
- Parlaklık: Metallere parlaklık sağlar.
Bu özelliklerin anlaşılabilmesi için metalik bağın oluşumuna ve elektron düzenine bakmak önemlidir.
Günlük Hayattan Basit Örnekler
- Bakır teller: Elektriği iletmek için sıklıkla bakır kullanırız. Bu, bakır atomlarının serbest elektronları sayesinde kolayca elektron akışına izin vermesindendir.
- Alüminyum folyo: Alüminyum levha hâline çok ince biçimde getirilebilir. Bu da metalik bağ yapısının metali kolayca dövülebilir kılması sayesindedir.
- Demir çivi: Demirin sert ve dayanıklı olması, demir atomlarının elektron bulutuyla oluşturduğu güçlü metalik bağ ile ilgilidir.
Elektron Deniz (Elektron Bulutu) Modeli
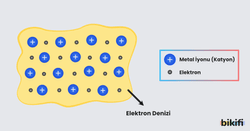
Metal atomlarında, değerlik elektronları (yani en dış katmandaki elektronlar) atom çekirdeğine gevşek bir şekilde bağlıdır. Bu elektronlar kolayca koparak “elektron denizi” veya “elektron bulutu” dediğimiz ortak bir alan içinde serbestçe hareket edebilir.
- Metal Katyonları: Metal atomları, değerlik elektronlarını bıraktığında pozitif yüklü iyonlar (katyonlar) hâline gelir.
- Serbest Elektronlar: Bırakılan elektronlar, katyonların çevresinde serbestçe hareket eden bir elektron bulutu oluşturur.
Metalik bağ, işte bu pozitif yüklü metal iyonları ile negatif yüklü elektron denizi arasındaki çekim kuvveti olarak açıklanır. Bu modeli anlamak, metallere ait iletkenlik ve şekil verilebilme özelliklerini kavramamızda yardımcı olur.
Metalik Bağın Oluşumu
Metalik bağ, Coulomb kuvveti adı verilen elektrostatik çekimle açıklanır. Pozitif ve negatif yükler birbirini çeker. Metal atomları değerlik elektronlarını kolaylıkla bırakarak pozitif yüklü iyonlara dönüşür ve bu iyonlar serbest elektronların oluşturduğu bulut tarafından sarılır. Bu çekimi basitçe Coulomb yasası ile ilişkilendirebiliriz:
Burada:
- elektrostatik kuvveti,
- ve yük miktarlarını,
- yükler arasındaki uzaklığı,
- ise Coulomb sabitini ifade eder.
Metalik bağda, metal katyonlarının pozitif yükünü, ise serbest elektronların negatif yük�ünü temsil eder. Aralarındaki uzaklık ( ) ve yük miktarları arttıkça çekim kuvveti de değişir.
Metalik Bağın Özelliklerine Etki Eden Faktörler
Metalik bağın gücü, yani katyonların elektron bulutu ile etkileşimi, farklı değişkenlere göre değişebilir:
- Metal Atomunun Çapı: Çap ne kadar küçükse çekirdek ile elektronlar arasındaki etkileşim daha güçlü olabilir.
- Değerlik Elektron Sayısı: Değerlik elektron sayısı arttıkça elektron denizi daha yoğun olur ve pozitif iyonlarla elektronlar arasındaki çekim artabilir.
- Katyon Yükü: Atom, ne kadar fazla elektron verip katyon yükü oluşturuyorsa çekim kuvveti de o kadar artar.
Bu etkenler, farklı metallerin erime noktası, kaynama noktası veya sertlik gibi özelliklerinde belirgin farklar oluşturur.
Örnek Metalik Bağ İncelemeleri
Farklı metallerin değerlik elektron sayıları farklıdır. Örneğin:
- Sodyum (Na): Tek değerlik elektronu ( ) vardır, kolayca pozitif yüklü katyona (Na⁺) dönüşür.
- Magnezyum (Mg): İki değerlik elektronu ( ) vardır, Mg²⁺ oluşturarak daha güçlü bir metalik bağ sergiler.
- Kalsiyum (Ca): İki değerlik elektronu ( ), benzer şekilde Ca²⁺ iyonu oluşturur.
- Alüminyum (Al): Üç değerlik elektronu ( ), Al³⁺ iyonu oluşturabilir ve daha yoğun bir elektron denizine sahiptir.
Bu metallerde metalik bağ, pozitif iyonlar ile serbest dolaşan elektronlar arasındaki çekime dayanır. Değerlik elektron sayısı arttıkça metalik bağ genellikle güçlenir ve metalin fiziksel özelliklerinde (erime noktası, sertlik vb.) değişimler gözlenir.