İki elementin birbirleriyle karıştırılması sonucunda, toplam iç enerji minimum olacak şekilde yeni atom düzenleri meydana gelmektedir. Fazlar, iç enerjinin minimum olmasını sağlayacak düzende oluşmaktadırlar. Kimyasal bileşim ve sıcaklığa bağlı olarak belirli şartlarda hangi fazların stabil olduğu (örneğin basınç sabit vb.) faz diyagramları ile belirlenmektedir. Faz diyagramları yardımıyla alaşımların hangi fazlardan oluştuğu, fazların bileşimi ve yüzde miktarları belirlenebilmektedir. Faz diyagramları tek bir elementi, ikili ve üçlü alaşımları incelerken kullanılabilir.
Faz diyagramlarını malzeme üretiminde, iç yapıları ve kararlılık bölgelerini saptamada, fiziksel kimyada denge hallerini bulmada ve en çok alaşımların elde edilmesinde kullanmaktayız.
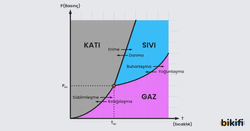
Tek bileşenli faz diyagramlarında kimyasal bileşim sabit tutulmakta (bu durumda faz diyagramı sadece saf maddeler için geçerli olmakta) ve sıcaklık ile basınç faz diyagramının değişkenlerini oluşturmaktadır. Söz konusu iki boyutlu diyagramlar aynı zamanda basınç-sıcaklık (P-T) diyagramları olarak nitelendirilmektedir. En basit faz diyagramı suyun basınç-sıcaklık diyagramı olarak gösterilebilir. Aşağıda suyun basınç-sıcaklık diyagramı verilmiştir.
Faz diyagramlarında 3 eğrinin kesiştiği ve grafikte de kırmızı olarak gösterilen noktaya “üçlü nokta” denilmektedir. Bu noktada sistem 273,16 K sıcaklığında ve 6.04x 10-3 atm basınç altında sadece bu noktada sistemin 3 fazı ( katı, sıvı, buhar) birbirleriyle dengede bulunduğu noktadır ve bu noktadan sıcaklık ve/veya basınçta olabilecek değişiklikle uzaklaşılması durumunda en azından fazlardan biri yok olur. Faz diyagramları sıcaklık ve basınç değerleri yardımıyla bize maddenin hangi fazda olduğunun anlaşılmasında işe yaramaktadır.