Atomların etrafındaki elektronlar orbitaller içerisinde bulunur. Farklı orbitaller farklı enerji seviyelerini simgeler. Bu demektir ki, 2s orbitalinde bulunan bir elektronun 1s orbitalindeki elektrondan daha fazla enerjisi vardır. Aynı şekilde 3p orbitalinde bulunan bir elektronun da 3s orbitalinde bulunan bir elektrondan daha fazla enerjisi bulunmaktadır.
Elektronların birbirleri arasında kovalent bağ yapması için elektronlarını ortaklaşa kullanmaları gerekmektedir. Enerji düzeyi uyuşmayan elektronlar (örneğin 3p’de bulunan bir elektronla 3s’de bulunan bir elektronun kovalent bağ yapması gerektiği bir durumda) böyle bir durumda orbitallerini eş seviyeye getirir. Orbitallerin eş seviyeye gelmesi durumuna hibritleşme ya da melezleşme denir. Oluşan yeni orbitallere de hibrit orbitalleri adı verilir. Aşağıdaki tablodan detaylarını görebilirsiniz.
Hibritleşmeler
Organik kimya konu olarak daha çok karbon atomuna odaklı olduğu için “s” ve “p” orbitalleri arasındaki hibritleşmeye dikkat edeceğiz. “s” ve “p” orbitalleri kendi arasında 3 çeşit hibritleşme yapabilir. Bunlar; “sp³”, “sp²”, “sp” hibritleşmeleridir.
| Durum | sp3 Hibritleşmesi | sp2 Hibritleşmesi | sp Hibritleşmesi |
|---|---|---|---|
| Temel Durum | |||
| Temel Durumun Orbital Gösterimi | |||
| Aktiflenmiş Durum | |||
| Aktiflenmiş Durumun Orbital Gösterimi | |||
| Aktiflenme Açıklaması | 1 tane s orbitali, 3 tane p orbitali ile hibritleşme yapmıştır. | 1 tane s orbitali, 2 tane p orbitali ile hibritleşme yapmıştır. 1 tane p orbitali hibritleşmeye katılmadı. | 1 tane s orbitali, 1 tane p orbitali ile hibritleşme yapmıştır. 2 tane p orbitali hibritleşmeye katılmadı. |
| Yeniden Düzenlenmiş Yapı | |||
| Son Durum | Üzerinde nokta bulunan orbitaller orbitalidir. | Üzerinde nokta bulunan orbitaller orbitalidir. | Üzerinde nokta bulunan orbitaller sp orbitalidir. |
| sp3 Hibritleşmesi | sp2 Hibritleşmesi | sp Hibritleşmesi |
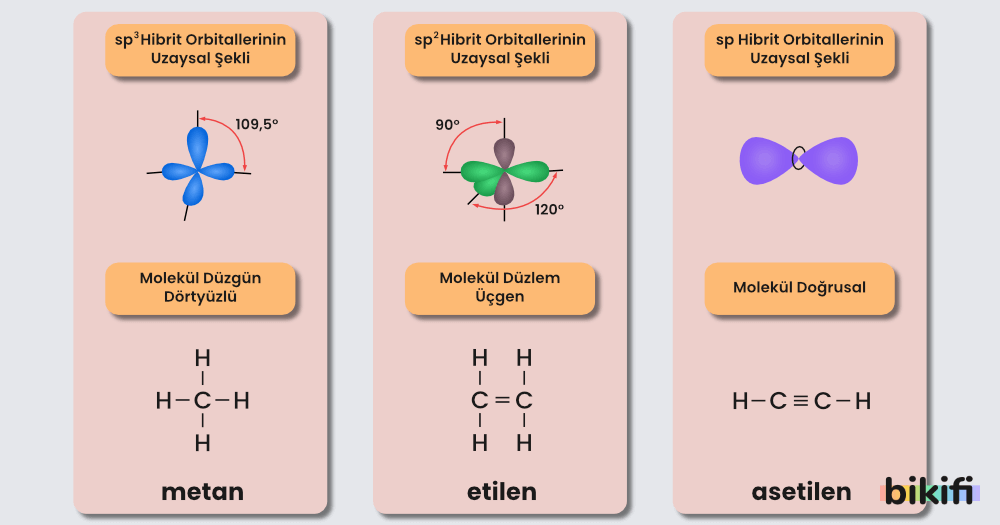
Sp³ Hibritleşmesi
Atomdaki bir s orbitaliyle üç p orbitalinin etkileşmesi sonucu meydana gelir. Örneğin; karbon atomu 2s1 ve 2p3 orbitallerini birleştirip 4 tane sp3 orbitali oluşturarak diğer atomların sp3 orbitalleriyle bağ yapabilir. Sp3 hibritleşmesi yapmış bir karbon atomu çift veya üçlü bağ yapamaz.
Sp2 Hibritleşmesi
Atomdaki bir s orbitaliyle iki p orbitalinin etkileşmesi sonucu meydana gelir. Sp2 hibritleşmesinde açıkta kalan bir p orbitali karbon atomunun diğer elementlerle çift bağ yapmasını sağlar.
Sp Hibritleşmesi
Atomdaki bir s orbitaliyle bir p orbitalinin etkileşmesi sonucu meydana gelir. Sphibritleşmesinde açıkta kalan iki adet p orbitali karbon atomunun diğer elementlerle üçlü bağ yapmasını sağlar.
Sigma ve Pi Bağları
- İki orbitalin bağ ekseni boyunca uç uca örtüşmesi sonucu oluşan bağlara sigma bağı, bağ eksenin dik olarak örtüşmesine pi bağı denir.
- Sigma bağlarında elektronlar atomun çekirdeğine daha yakın bir konumda bulunduğu için pi bağlarından daha güçlüdür.
- Sigma bağı oluşmadan pi bağı oluşmaz. İki atom arasında bir bağ varsa bu sigma bağı, birden fazla bağ varsa biri sigma diğerleri pi bağıdır.
Örnek olarak BeCl2 bileşiğinin nasıl meydana geldiğine bakalım. BeCl2 bileşiğinin geometrik yapısı çizgisel, bağ açıları ise 180o’dir. “Cl-Be-Cl” şeklindedir.
Berilyum, 2. periyot ve 2A grubu elementidir. Atom numarası 4’tür. Berilyumun elektron dağılımı; Be:1S² 2S² 2Px° 2Py° 2Pz° şeklindedir. Burada hem 1S hem de 2S orbitalleri dolu görünmektedir. Ancak 2. Enerji düzeyinde 3 tane boş 2P orbitali vardır. 2S deki elektronlardan biri küçük bir enerji alarak 2P orbitallerinden birine atlayabilir. Bu olaya uyarılma adı verilir. Uyarılma sonunda elektronlar ancak aynı enerji yörüngesindeki boş orbitallere atlayabilirler. 1s’den 2p’ye elektron atlaması mümkün olmaz.
Berilyumun uyarılması ile oluşan iki yarı dolmuş orbitalin enerji düzeyleri farklıdır. Eğer berilyum bu haliyle iki Cl atomu bağlarsa, bağlardan biri S-P bağı, diğeri P-P bağı olacaktır. Bu durumda BeCl2 deki bağlar birbirinden farklı olacaktır. Ancak, yapılan deneyler göstermiştir ki, Be-Cl bağlarının ikisi birbiriyle özdeştir. Öyleyse, Be atomu, bağ yapmadan önce ya da tam bağ yaparken 2S ve 2P orbitalleri karışarak yeni bir orbital sistemi oluşturmuştur. Bu olay şu şekilde meydana gelir.
- 2S orbitalinin enerji düzeyi biraz artar, 2P orbitalinin enerji düzeyi biraz azalır ve iki orbital aynı enerji düzeyine gelir.
- Aynı enerji düzeyine gelen bu iki orbital ne 2S ne de 2P orbitalidir. Bunlar karışarak sp ile gösterilen iki melez orbital oluşturmuşlardır.
- Melez orbitaller bir s ve bir p orbitalinin karışmasıyla oluştukları için bu olaya sp melezleşmesi adı verilir. Olay aşağıdaki şekille daha iyi açıklanabilir.
Molekül Geometrisi – VSEPR Modeli
Küçük moleküllü bileşiklerin geometrilerini tahmin etmek için VSEPR (Değerlik Kabuğu Elektron Çiftleri İtme Kuramı) kullanılır. VSEPR kuramında molekül geometrisini ortaklanmış ve ortaklanmamış elektronlar belirler. VSEPR kuramının uygulanması:
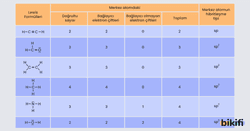
- Molekülün Lewis yapısı yazılır ve merkez atomu üzerinde kaç elektron çifti (ortaklanmış ve ortaklanmamış) olduğu belirlenir.
- Elektron çiftlerinin dizilişi belirlenir.
- Atomlar yerleştirilerek molekülün biçimi sınıflandırılır.
- Ortaklanmamış elektron çiftlerinin birbirinden ve bağ yapan çiftlerden en uzakta bulunabilmeleri için molekül şekli bir miktar bozulur.
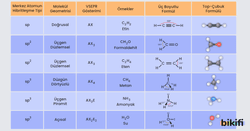
VSEPR modelinde;
- A ; merkez atomu,
- X ; merkez atoma bağlı atomları,
- E ; ise ortaklanmamış elektron çiftlerini sembolize eder.
Örnek verecek olursak BeH2‘nin VSEPR gösterimi AX2 şeklindedir. Örnek olarak aşağıdaki tabloyu inceleyebilirsiniz.