İncelenmek üzere seçilen sınırlı bir bölüme sistem denir. Sistemin sınırları yapılmak istenen gözleme göre şekillenir; bir kozmolog için sistem galaksi kadar büyük olabileceği gibi bir biyolog için sistem bir hücre kadar küçük de olabilir. Sistem dışında kalan evren parçasına çevre denir.
- Sistem: Kimyacılar için özellikle kimyasal ve fiziksel değişimlere katılan maddeleri kapsar.
- Çevre: ise sistemin dışında kalan evrenin diğer kısmıdır. Başka bir değişle çevre sistemin içinde bulunduğu yerdir.
- Evren: İncelenen olayların gerçekleştiği sistem ve sistemin bulunduğu çevre bir bütün olarak evreni oluşturur.
Kimyasal olayların hepsinde bir enerji değişimi gözlemlemek mümkündür. Enerji; kinetik enerji, potansiyel enerji, ısı enerjisi vb. gibi birden çok çeşitten oluşmaktadır ve enerjiler birbirleri arasında dönüşebilir. Her türlü enerji kimyasal olarak iş yapabilme becerisine sahiptir. Kimyasal olarak iş, bir süreçten kaynaklanan enerji değişimi olarak tanımlanır.
Kimyasal tepkimelerin çok büyük bir kesiminde ısı enerjisinde bir değişim olmaktadır. Kimya biliminde bu durum ile ilgili olan konularla termokimya ilgilenir.
Sistemlerin çevre ile arasında ısı alışverişi, madde alışverişi gibi aktiviteler gözlemlenebilir. Ayrıca sistemlerin bazı özelliklerinin (sıcaklık, basınç, hacim gibi özellikler) sabit olabildiği ortamlar da yaratılabilmektedir.
Sistemlerin Çevre ile İlişkisine Göre Sınıflandırılması
Sistemler, içinde bulundukları çevre ile madde ve enerji alışverişi durumuna göre üçe ayrılır.
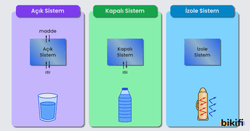
Açık Sistemler
Çevresi ile hem madde hem de ısı değişimi yapabilen sistemlere açık sistem denir. Yukarıdaki görselde bulunan içi kahve dolu fincan açık sisteme örnek verilir.
Kapalı Sistemler
Çevresi ile madde alışverişi yapmayan sadece ısı alışverişi yapan sistemlere kapalı sistem denir. Ağzı kapalı bir pet şişe kapalı sisteme bir örnektir.
Yalıtılmış (İzole) Sistemler
Çevresi ile madde ve ısı değişimi yapmayan sistemlere yalıtılmış (izole) sistem denir. İçi dolu termostaki su teorik olarak izole bir sistemdir.
Sistemlerin Sabit Olan Değişkene Göre Sınıflandırılması
Sistemler sıcaklık basınç ve hacim değişkenlerinin sabitlik durumuna göre 3 şekilde sınıflandırılır.
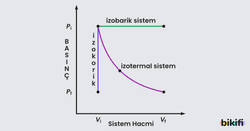
İzotermal Sistem
Sabit sıcaklıkta bulunan açık sistemlere izotermal sistemler denilmektedir. Bu sistemlerde çevre ile ısı alışverişi çok hızlı olduğundan sıcaklığın sabit olduğu varsayımı hakimdir. İnsan vücudu çoğu zaman (hastalık dönemleri hariç) izotermal sistem içerisinde değerlendirilir.
İzokorik Sistem
Hacmin sabit tutulduğu sistemlere izokorik sistemler denilir. İzokorik bir sistemde iç enerji değişimi açığa çıkan veya soğrulan ısıya eşittir.
İzobarik Sistem
Basıncın sabit kaldığı sistemlere izobarik sistemler denilmektedir. Bu tür sistemlerde hem mekanik iş hem de ısı değişimi gözlemlenir. Çoğu kimyasal tepkime atmosfer basıncı altında gerçekleştiği için izobarik bir sistem içerisinde bulundukları varsayımı yapılabilir.